Algunas características del agua
El agua, uno de los cuatro componentes fundamentales presentes en los alimentos, es extremadamente importante tanto por su necesidad vital desde el punto de vista nutricional como por su influencia en las propiedades físicas, químicas y microbiológicas del alimento en el que se encuentra.
Para comprender por qué el agua es tan importante, es necesario conocer sus principales propiedades y características.
El agua es un compuesto formado por la unión covalente de dos átomos de hidrógeno con un átomo de oxígeno.
La forma de la molécula de agua y el hecho de que el oxígeno sea más electronegativo que el hidrógeno en los enlaces O–H confieren al agua un carácter polar, con extremos negativos y positivos. Algunas de las características del agua se presentan a continuación;
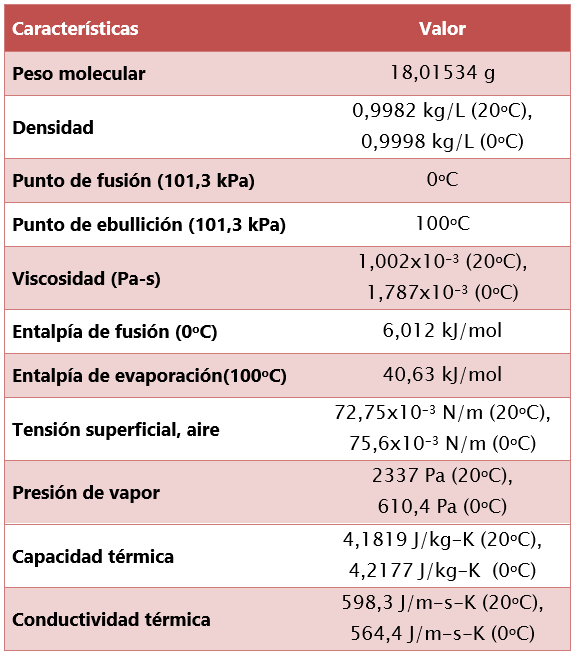
Entre las moléculas de agua se forman enlaces de hidrógeno, específicamente entre el oxígeno de una molécula de agua y el hidrógeno de una molécula vecina.
El hecho de que las moléculas de agua en un sistema tridimensional formen enlaces de hidrógeno entre sí explica la alta capacidad calorífica del agua, su tensión superficial, su punto de fusión, su entalpía de vaporización y de fusión, así como sus elevadas fuerzas de adhesión y cohesión.
La elevada adhesión y cohesión del agua le permiten adherirse fácilmente a sustancias extrañas y humedecerlas, así como desplazarse contra la gravedad, como ocurre en los vasos capilares de las plantas.
El hecho de que el estado sólido del agua (hielo) tenga una densidad menor que su estado líquido también está relacionado con el número de enlaces de hidrógeno intermoleculares formados y con la longitud de dichos enlaces.
La presencia de extremos positivo y negativo en la molécula de agua permite que los compuestos iónicos se disuelvan bien en agua. Además, compuestos no iónicos pero polares, como los azúcares y los alcoholes simples, también pueden disolverse en agua.
El efecto se debe principalmente a la formación de enlaces de hidrógeno entre grupos polares (entre el oxígeno del agua y el grupo carbonilo del compuesto disuelto).
Formas de agua en los alimentos
Todos los alimentos contienen agua en mayor o menor cantidad. Por ejemplo, la carne contiene aproximadamente un 70 % de agua, mientras que la leche contiene alrededor de un 87 %. En la siguiente tabla se presenta el contenido de agua de algunos alimentos;
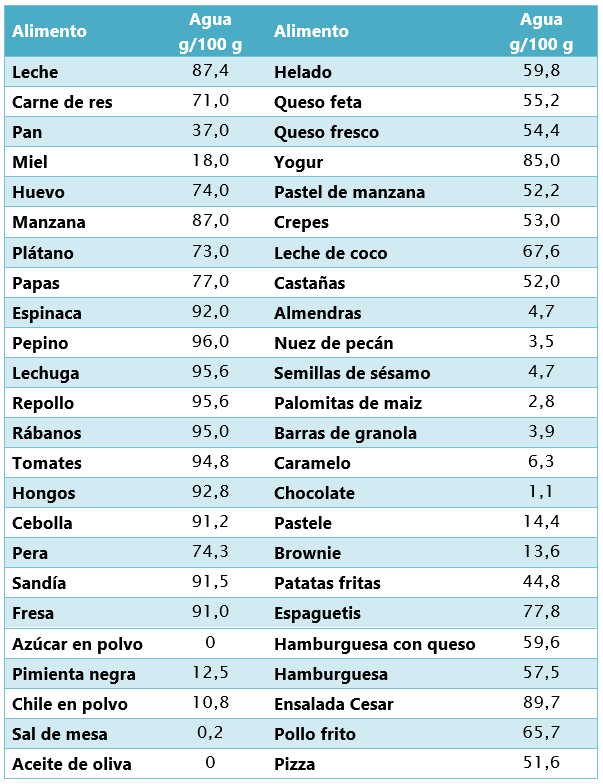
Sin embargo, no toda el agua presente en los alimentos se comporta como agua libre ni posee todas las propiedades del agua. El agua se encuentra en los alimentos en cinco formas diferentes, que se describen a continuación;
1. Agua Estructural: Agua que forma parte de componentes distintos del agua. No posee carácter disolvente, no se congela a –40 °C y su actividad de agua es cero. Constituye un porcentaje muy pequeño del agua total presente en los alimentos.
2. Agua Vicinal: Agua unida a compuestos con fuertes grupos polares hidrofílicos. No posee carácter disolvente, no se congela a –40 °C y su actividad de agua es cero. En cantidades elevadas, puede rodear los grupos polares hidrofílicos en una sola capa.
3. Agua Multicapa: Agua unida al agua vicinal. Debido a su proximidad a componentes distintos del agua, puede presentar parcialmente las características del agua pura. Una gran parte no se congela a –40 °C y puede presentar propiedades disolventes.
4. Agua Libre: Agua presente en el alimento alejada de los componentes no acuosos y que interactúa únicamente con otras moléculas de agua. Las características de esta agua se asemejan a las de una solución salina diluida. El agua libre puede congelarse por debajo de 0 °C y presentar propiedades disolventes.
5. Agua Atrapada: Agua situada entre grandes macromoléculas. Puede eliminarse fácilmente mediante secado o congelarse con facilidad. El agua presente en geles de pectina y almidón, así como en tejidos animales y vegetales, es un ejemplo de agua atrapada.
A partir de esta clasificación, puede afirmarse que no toda el agua contenida en un alimento presenta las propiedades del agua libre. Esto significa que no toda el agua presente en un alimento está “disponible” para reacciones físicas y químicas ni para la actividad de los microorganismos.
Por lo tanto, además de la cantidad total de agua contenida en un alimento, es extremadamente importante conocer qué proporción de esa agua presenta realmente las propiedades del agua, tanto para la conservación como para el procesamiento de los alimentos. Una de las razones por las que dos alimentos con el mismo contenido de agua pueden tener diferentes vidas útiles es la distinta proporción de las formas de agua que contienen.
El parámetro conocido como “actividad de agua” se utiliza para medir la “disponibilidad” del agua en los alimentos. La actividad de agua se define como la relación entre la presión de vapor del agua en un alimento y la presión de vapor del agua pura a la misma temperatura.
El símbolo de la actividad del agua es “aw.” La actividad de agua varía entre 0 y 1 y se expresa sin unidades. Por ejemplo, la actividad de agua del agua pura es 1; la de la miel es aproximadamente 0,60 y la de la leche en polvo es aproximadamente 0,2.
La importancia de la actividad de agua puede explicarse de la siguiente manera;
La mayoría de las bacterias patógenas requieren un medio con una actividad de agua de al menos 0,91 aw para mantener sus funciones vitales. Si la actividad de agua de un alimento es inferior a 0,91, o si se reduce por debajo de este valor mediante procesos como el secado o la concentración, el alimento deja de ser apto para el crecimiento de la mayoría de las bacterias patógenas. Por lo tanto, dichas bacterias ya no pueden causar daño al alimento (este tema se abordará con mayor detalle en la sección de microbiología de los alimentos).
Desde el punto de vista de las reacciones químicas, la reacción de Maillard alcanza su velocidad máxima en valores de aw entre 0,65 y 0,70. En alimentos que contienen altas cantidades de aminoácidos y azúcares reductores, el valor de la actividad de agua es particularmente importante. De manera similar, la cantidad de vitamina C presente en un alimento está estrechamente relacionada con su actividad de agua. De hecho, a medida que aumenta la actividad de agua, también aumenta la velocidad de degradación de la vitamina C.
No obstante, debe tenerse en cuenta que, aunque el parámetro de actividad de agua se utiliza eficazmente a temperaturas superiores al punto de congelación, pierde en gran medida su validez a temperaturas inferiores al punto de congelación. (Para información detallada ver Actividad del Agua en los Alimentos; Definición, Importancia y Efectos)
Otro concepto importante en la relación entre los alimentos y el agua es la “humedad de equilibrio.” Como es sabido, los alimentos absorben humedad del entorno o liberan humedad al mismo.
En un mismo ambiente, una galleta puede absorber humedad y reblandecerse, mientras que un tomate puede perder humedad y secarse. Después de un cierto tiempo, el contenido de humedad del alimento y el del entorno alcanzan el equilibrio y se estabilizan.
El punto en el que se alcanza el equilibrio se denomina “contenido de humedad en equilibrio” y se expresa en unidades de g de humedad/g de materia seca. Naturalmente, el contenido de humedad en equilibrio varía según la temperatura y la humedad relativa del entorno.
Cuando el proceso mediante el cual un alimento alcanza su contenido de humedad en equilibrio como resultado del intercambio de humedad con el entorno se representa gráficamente, se obtienen las “isotermas de sorción.” La representación gráfica de la fase en la que un alimento completamente seco gana humedad del entorno hasta alcanzar el equilibrio se denomina “isoterma de adsorción.”
La representación gráfica de la fase en la que un alimento húmedo pierde humedad hasta alcanzar el equilibrio con la humedad ambiental se denomina “isoterma de desorción.” Los datos de las isotermas de sorción se obtienen experimentalmente. El contenido de humedad en equilibrio y las isotermas de sorción son extremadamente importantes en el almacenamiento y la conservación de los alimentos.
Para obtener información detallada sobre la importancia del agua para la salud y las necesidades diarias de agua, consulte. Funciones del Agua en el Cuerpo y Necesidad Diaria de Agua