Le sujet de la structure cyclique et de l’isomérie des monosaccharides est l’un des sujets les plus difficiles en chimie alimentaire, car il contient énormément de détails, comprend de nombreux termes et, en particulier, parce que les différents isomères sont très souvent confondus les uns avec les autres.
Compte tenu de l’importance du sujet, dans cet article, je vais essayer d’expliquer de manière détaillée et compréhensible à la fois les structures cycliques et l’isomérie des monosaccharides. Dans la première partie de l’article, la structure cyclique des monosaccharides est expliquée. Dans la seconde partie, présentée plus bas, j’essaierai d’expliquer l’isomérie des monosaccharides et la classification de cette isomérie.
1. La structure cyclique des monosaccharides
Dans la projection de Fischer, la structure des monosaccharides apparaît sous la forme d’une chaîne linéaire (voir Glucides; Monosaccharides, disaccharides et polysaccharides). Cependant, bien que cette structure linéaire théorique soit correcte, les monosaccharides contenant 5 atomes de carbone (C) ou plus dans leur chaîne se trouvent sous forme cyclique dans les conditions naturelles.
Comme on le sait, les monosaccharides – qu’il s’agisse d’aldoses ou de cétoses – contiennent dans leur structure un groupe carbonyle (C=O) et plus d’un groupe hydroxyle (-OH). Comme on peut s’en souvenir de la chimie organique, le groupe carbonyle est électrophile.
Dans ces conditions, l’un des groupes hydroxyles présents dans la structure des monosaccharides (généralement les groupes -OH liés aux atomes de carbone C5 ou C4) effectue une attaque nucléophile sur le groupe carbonyle de la même chaîne (la paire libre d’électrons de l’atome d’oxygène du groupe -OH attaque l’atome de carbone du groupe carbonyle).
En conséquence, une liaison covalente (C–O) se forme entre l’oxygène lié au groupe hydroxyle et l’atome de carbone du groupe carbonyle, et la structure linéaire se transforme en structure cyclique.
Pour le décrire dans le langage de la chimie, le groupe carbonyle et le groupe hydroxyle subissent une réaction intramoléculaire, formant un hémiacétal ou un hémicétal.
Dans la projection de Fischer, les formes D et L des monosaccharides peuvent être représentées facilement dans la structure linéaire. Cependant, les formules de Haworth sont utilisées afin de représenter de manière compréhensible la structure cyclique et les nouvelles formes stéréoisomériques formées. Les formules de Haworth sont utilisées depuis plus de 100 ans pour représenter clairement sur papier la structure cyclique tridimensionnelle. Dans la formule de Haworth, le plan est considéré comme horizontal. Les liaisons dessinées avec des traits plus épais que les autres indiquent que cette partie de la molécule est plus proche de l’observateur.
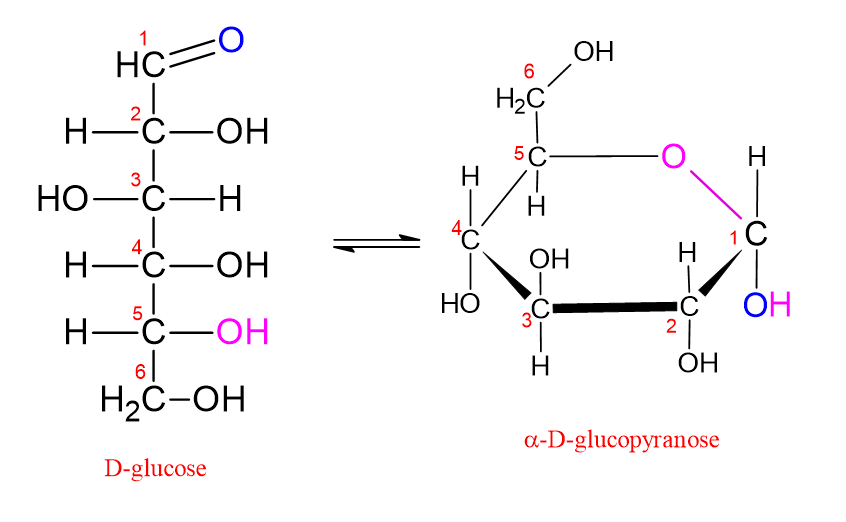
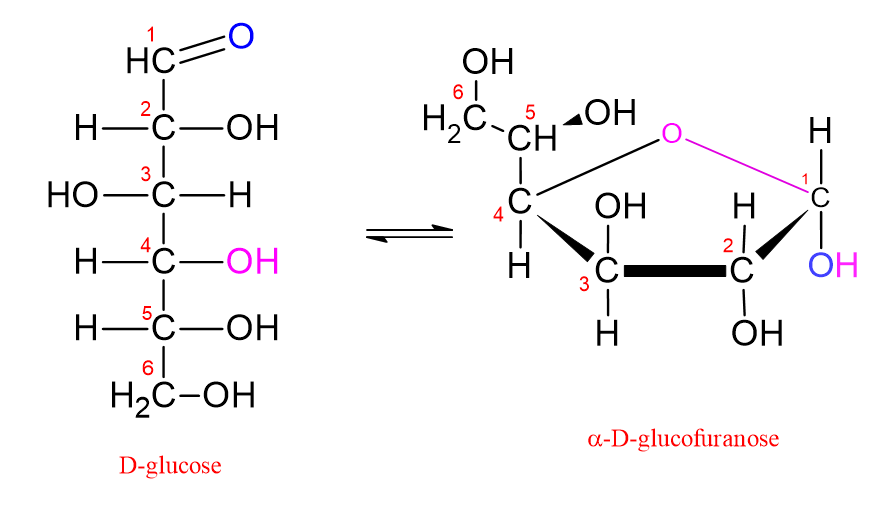
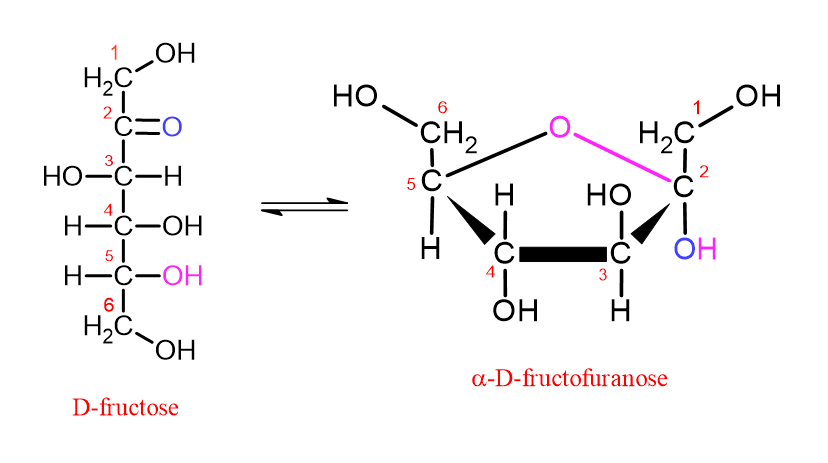
En général, les sources de référence expliquent les structures cycliques des monosaccharides avec des formulations telles que “les monosaccharides possédant 5 atomes de carbone ou plus présentent une structure cyclique en milieu aqueux ou en solution.” Cependant, cette explication est très sujette à mauvaise interprétation et est trompeuse dans le sens qu’elle suggère.
Car cette affirmation peut laisser penser que les monosaccharides présentent une structure cyclique uniquement en milieu aqueux, tandis qu’à l’état cristallin et sec ils resteraient sous forme linéaire ouverte. En réalité, les monosaccharides possédant 5 atomes de carbone ou plus existent sous forme cyclique dans presque toutes les conditions et dans presque tous les environnements. Pour prendre le glucose comme exemple, le glucose est produit dans la plante sous forme ouverte, mais dans l’environnement cellulaire il adopte immédiatement la structure cyclique, quelques millisecondes seulement après sa formation.
D’autre part, la forme linéaire ouverte et la forme cyclique des monosaccharides sont dans un état constant d’interconversion. Par exemple, dans une solution aqueuse de glucose, la molécule de glucose passe continuellement d’une forme à l’autre entre la forme linéaire ouverte et la forme cyclique. Cependant, à un moment donné, plus de 99 % du glucose en solution se trouve sous forme cyclique, tandis que moins de 0,1 % du reste se trouve sous forme linéaire ouverte. À l’état cristallin sec du glucose, presque toutes les molécules sont sous forme cyclique, et une transition vers la forme linéaire ouverte, comme observée en milieu aqueux, ne se produit pas. Dans des structures plus grandes telles que le saccharose et l’amidon, le glucose est également présent sous forme cyclique.
Plusieurs questions peuvent se poser ici. Essayons d’y répondre brièvement:
Question 1: Pourquoi les monosaccharides possédant 5 atomes de carbone ou plus peuvent-ils former des structures cycliques, alors que ceux ayant moins d’atomes de carbone ne le peuvent pas ?
Réponse: Cela est entièrement lié à la stabilité et à l’adéquation structurale. Les monosaccharides possédant 3 atomes de carbone ne sont pas suffisamment longs pour former une structure cyclique. Dans les monosaccharides possédant 4 atomes de carbone, la structure cyclique qui se formerait ne serait pas stable en raison de la forte contrainte intramoléculaire.
Question 2: Pourquoi le groupe hydroxyle n’attaque-t-il pas le groupe carbonyle d’un monosaccharide voisin, mais attaque-t-il son propre groupe carbonyle?
Réponse: La raison la plus importante est l’absence de concentration efficace. À l’intérieur de la molécule, les groupes carbonyle et hydroxyle sont toujours proches l’un de l’autre et dans la bonne position géométrique. Pour qu’un groupe appartenant à une autre molécule soit proche, au bon angle et avec la bonne énergie, il faut attendre que ces conditions soient réunies; cela constitue un désavantage considérable. En outre, si une telle liaison se formait, elle donnerait naissance à une molécule très grande et irrégulière, ce qui n’est pas une voie favorable.
Dans les monosaccharides possédant plus de 5 atomes de carbone, il existe deux groupes hydroxyles (-OH) situés à une distance appropriée pour se lier à l’atome de carbone du groupe carbonyle (C=O) lors de la formation du cycle : les groupes hydroxyles liés aux carbones C4 et C5.
Expliquons cela à travers le glucose, qui contient 6 atomes de carbone dans sa structure: dans le glucose, le groupe carbonyle (C=O) est situé sur le premier carbone (C1). Si le groupe hydroxyle lié au carbone C5 de la chaîne attaque le carbone carbonylé, un cycle à six chaînons se forme. Cela est appelé un “cycle pyranose.” Ce nom lui a été donné parce qu’il ressemble à la molécule de pyrane, qui est une structure cyclique oxygénée à six chaînons.
En outre, le groupe hydroxyle du carbone C4 du glucose est également à une distance appropriée pour réagir avec le carbone C1. Si le groupe hydroxyle lié au carbone C4 attaque le carbone carbonylé, alors un cycle à cinq chaînons se forme. Cela est appelé un “cycle furanose.” Ce nom lui a été donné parce qu’il ressemble à la molécule de furane, qui est une structure cyclique oxygénée à cinq chaînons.
En conséquence, deux types différents de cycles peuvent être observés dans les monosaccharides:
1. Pyranose; une structure cyclique à six chaînons dont l’un des membres est un atome d’oxygène
2. Furanose; une structure cyclique à cinq chaînons dont l’un des membres est un atome d’oxygène
Les structures cycliques pyranose et furanose de certains monosaccharides sont présentées ci-dessous;
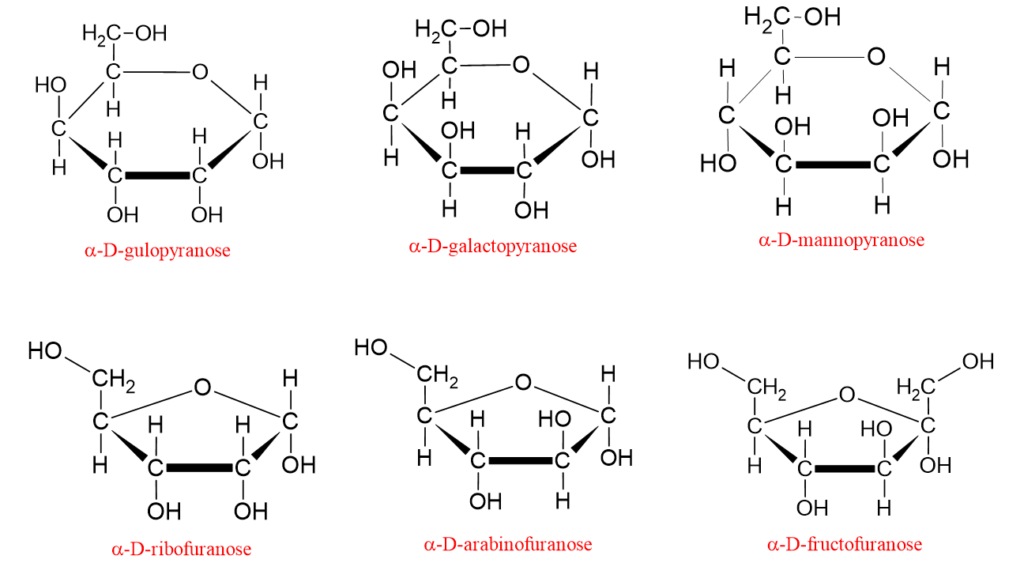
À ce stade, la question suivante peut venir à l’esprit: pourquoi seules des structures cycliques à 5 et 6 chaînons sont-elles observées dans les monosaccharides?
Réponse: Lors de la formation du cycle dans les monosaccharides, des cycles de différentes tailles peuvent théoriquement se former. Cependant, les cycles les plus fréquemment rencontrés dans la nature sont les cycles à cinq et six chaînons. La raison principale en est que les cycles de ces tailles sont chimiquement très stables.
Comme on peut s’en souvenir de la chimie organique, la stabilité des cycles est largement liée aux angles de liaison et à la contrainte intramoléculaire. Lorsque les atomes de carbone présentent une hybridation sp³, l’angle de liaison idéal est d’environ 109,5°. Dans les très petits cycles, cet angle est fortement déformé, et une forte contrainte apparaît à l’intérieur de la molécule.
Par exemple, dans les cycles à trois ou quatre chaînons, les angles de liaison s’écartent considérablement de la valeur idéale. Pour cette raison, ces cycles possèdent une énergie élevée et sont instables. En revanche, dans les cycles à cinq et six chaînons, les angles de liaison sont plus proches de l’idéal et la contrainte intramoléculaire est beaucoup plus faible. Par conséquent, ces cycles sont considérés comme plus stables.
Dans les cycles comportant plus de six membres, la contrainte angulaire n’est généralement pas un problème majeur. Cependant, lorsque ces cycles se forment, il devient plus difficile pour la chaîne de se refermer dans la bonne position. En d’autres termes, la probabilité que les extrémités de la molécule se rejoignent avec le bon angle et à la bonne position diminue. Cela rend la formation du cycle moins favorable sur le plan cinétique. En outre, comme les grands cycles sont généralement plus flexibles, des contraintes supplémentaires peuvent également apparaître dans certaines conformations.
Pour le dire brièvement:
• Les cycles comportant moins de 5 membres ne sont pas stables en raison de la contrainte angulaire.
• Les cycles à cinq et six membres sont les structures cycliques les plus stables.
• Les cycles comportant plus de 6 membres présentent une faible probabilité de fermeture et sont sujets à des contraintes supplémentaires.
Le tableau ci-dessous présente la tendance générale concernant la structure cyclique prédominante selon le type de monosaccharide;
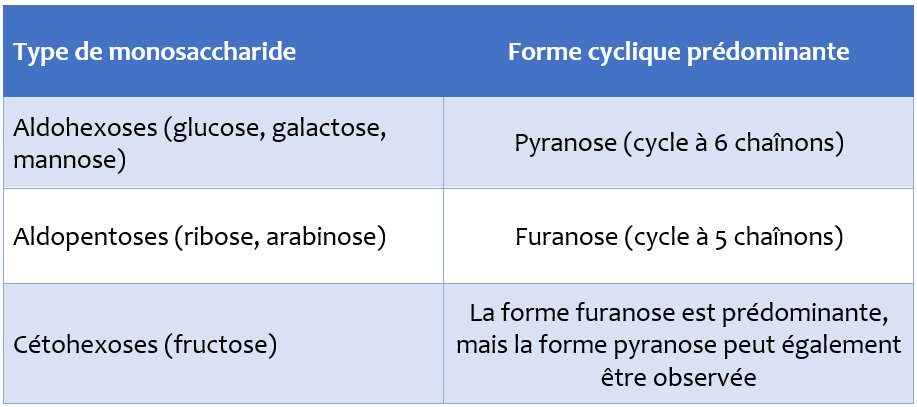
Ce tableau n’est pas une règle absolue, mais il montre une forte tendance. En solution, les monosaccharides existent dans un état d’équilibre dynamique entre différentes formes cycliques. Ainsi, en plus de la forme cyclique prédominante, d’autres types de cycles peuvent également être présents en faibles proportions. Cependant, chez la plupart des monosaccharides, cet équilibre favorise clairement une seule forme cyclique.
La structure cyclique entraîne également l’apparition d’un nouveau centre chiral. En poursuivant avec l’exemple du glucose, lorsque le glucose forme une structure pyranose, le carbone C1 qui contient le groupe carbonyle devient lui aussi un nouveau centre chiral (également appelé carbone asymétrique ou carbone anomérique).
Dans la structure linéaire du glucose, la chiralité des carbones est la suivante:
• C1: non chiral
• C2: centre chiral
• C3: centre chiral
• C4: centre chiral
• C5: centre chiral
• C6: non chiral
Lors de la détermination de la configuration de la molécule dans la structure linéaire, le carbone chiral possédant le numéro de carbone le plus élevé est pris comme référence. Dans ce cas, si le groupe hydroxyle (-OH) du carbone C5 du glucose se trouve à droite, cela est exprimé comme la configuration D; s’il se trouve à gauche, cela est exprimé comme la configuration L.
Cependant, avec le passage à la structure cyclique, le carbone C1 devient également chiral (ce carbone est désormais appelé carbone anomérique). Ainsi, deux possibilités de configuration supplémentaires apparaissent dans la structure cyclique. Selon la position du groupe hydroxyle (-OH) lié à cet atome de carbone chiral nouvellement formé, deux nouvelles formes stéréoisomériques apparaissent dans la structure cyclique: α (alpha) et β (bêta).
Dans la projection de Fischer, les groupes hydroxyles représentés du côté droit de la molécule sont représentés du côté inférieur de la molécule dans la formule de Haworth. Ceux représentés du côté gauche dans la projection de Fischer sont représentés du côté supérieur dans la formule de Haworth. Dans la formule de Haworth, si le groupe hydroxyle lié au carbone anomérique (C1) est représenté en dessous, la molécule est appelée forme α. Si le groupe hydroxyle lié au carbone anomérique (C1) est représenté au-dessus, la molécule est appelée forme β. Cela est montré dans la figure ci-dessous;
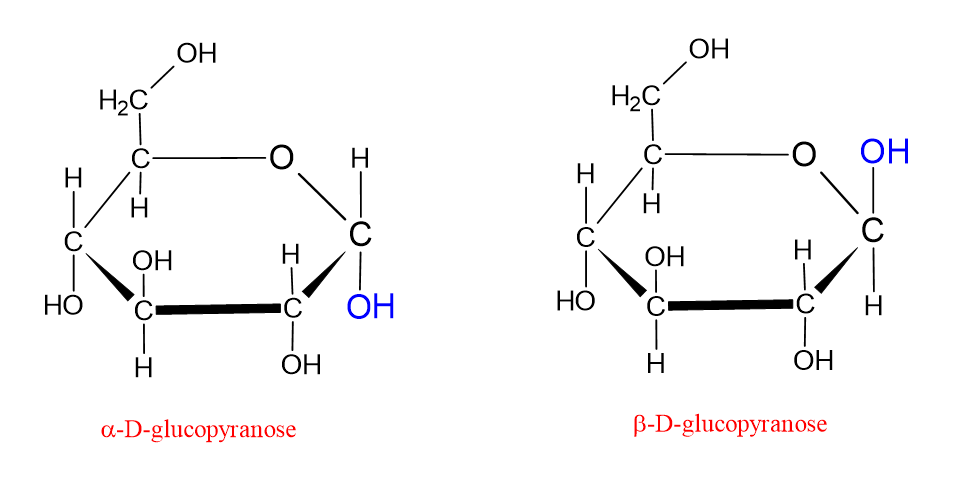
Les projections de Haworth sont extrêmement utiles pour représenter clairement la structure cyclique des monosaccharides. Cependant, cette représentation ne reflète pas complètement la véritable géométrie tridimensionnelle de la molécule. Dans la formule de Haworth, le cycle est dessiné comme un pentagone ou un hexagone plat. En réalité, cependant, les atomes de carbone présentent une hybridation sp³ et des angles de liaison d’environ 109,5°. Pour cette raison, les molécules ne peuvent pas former une structure cyclique parfaitement plane. Afin de rapprocher les angles de liaison de la valeur idéale et de réduire la contrainte intramoléculaire, la molécule adopte certaines conformations dans l’espace.
Les cycles furanose à cinq chaînons adoptent généralement des conformations en enveloppe et en torsion, tandis que les cycles pyranose à six chaînons se trouvent dans la nature principalement sous les conformations chaise et bateau. La raison principale de l’apparition de ces conformations est de rapprocher les angles de liaison de l’angle tétraédrique idéal et de réduire la contrainte intramoléculaire. Les différentes conformations formées par les monosaccharides sont présentées ci-dessous;
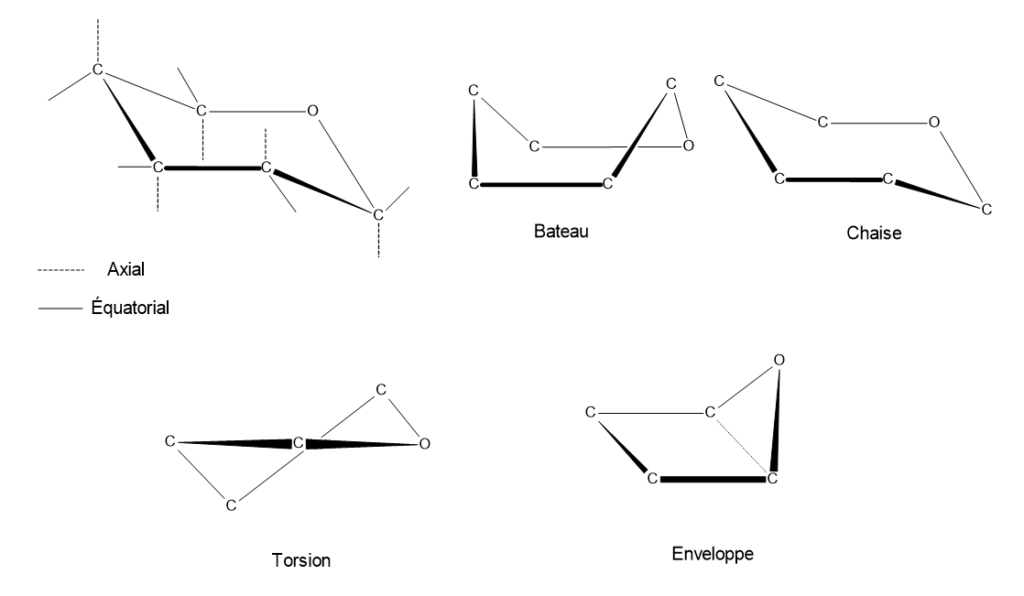
Dans la conformation chaise, les groupes liés à chaque atome de carbone du cycle peuvent occuper deux positions différentes dans l’espace: axiale et équatoriale. Les liaisons axiales sont orientées approximativement perpendiculairement au cycle, vers le haut ou vers le bas. Les liaisons équatoriales s’étendent vers l’extérieur du cycle dans une direction approximativement parallèle au plan du cycle.
En général, la position équatoriale est plus stable. La raison est que les groupes volumineux en position axiale créent une répulsion stérique avec les autres groupes axiaux du cycle (interactions 1,3-diaxiales). Pour cette raison, de petits atomes comme l’hydrogène peuvent occuper la position axiale, mais les groupes plus volumineux préfèrent la position équatoriale.
En résumé, on peut affirmer ce qui suit: dans la conformation chaise des cycles monosaccharidiques à six chaînons, la préférence des groupes volumineux pour la position équatoriale réduit les interactions stériques intramoléculaires et augmente la stabilité de la structure.
Dans la conformation chaise du β-D-glucopyranose, presque tous les groupes hydroxyles sont en position équatoriale, tandis que seuls les atomes d’hydrogène occupent des positions axiales. Cela réduit fortement la contrainte stérique intramoléculaire et rend la structure très stable. Par conséquent, le β-D-glucopyranose est la forme la plus stable du glucose et celle qui est présente dans la plus grande proportion en solution.
À ce stade, nous pouvons dire que nous avons terminé la structure cyclique des monosaccharides. Il reste maintenant l’explication de la rotation optique et de la mutarotation dans les monosaccharides.
1.1. Rotation optique et mutarotation dans les monosaccharides
Comme les monosaccharides contiennent plus d’un atome de carbone chiral, ils sont optiquement actifs. Les molécules optiquement actives possèdent la propriété de faire tourner la lumière polarisée plane dans une certaine direction. Le phénomène de modification de la direction de la lumière polarisée est appelé rotation optique.
Deux stéréoisomères différents d’une molécule optiquement active peuvent souvent présenter des propriétés physiques et chimiques similaires. Cependant, la direction et l’angle selon lesquels ces deux stéréoisomères font tourner la lumière polarisée leur sont propres. Par conséquent, l’activité optique est fréquemment utilisée pour distinguer les stéréoisomères d’une molécule.
Si une molécule fait tourner la lumière polarisée dans le sens horaire, elle est appelée positive (+) ou dextrogyre; si elle la fait tourner dans le sens antihoraire, elle est appelée négative (−) ou lévogyre.
Un point important ici est que ces signes ne peuvent pas être prédits de manière fiable simplement en observant la structure de la molécule. La direction dans laquelle une molécule fait tourner la lumière polarisée est généralement déterminée expérimentalement à l’aide de mesures réalisées avec un appareil appelé polarimètre. Ainsi, le signe (+) ou (−) placé devant le nom d’une molécule n’indique pas une prédiction théorique, mais plutôt une propriété déterminée expérimentalement.
Un autre point important concernant la rotation optique est qu’elle ne doit pas être confondue avec la désignation D et L. Le système D et L exprime la configuration de la molécule et est déterminé selon la position d’un carbone chiral spécifique dans la projection de Fischer. En revanche, les signes (+) et (−) indiquent la direction dans laquelle la molécule fait tourner la lumière polarisée. Il n’existe donc pas de relation directe entre la configuration D ou L et la direction de la rotation optique. Par exemple, le glucose est généralement exprimé sous la forme D-(+)-glucose, tandis que le fructose peut être représenté sous la forme D-(−)-fructose. Comme on peut le voir, bien que les deux molécules soient dans la configuration D, leurs directions de rotation optique sont différentes.
Enfin, lors de la dénomination d’une molécule, l’écriture du signe (+) ou (−) n’est souvent pas obligatoire. Dans l’identification des monosaccharides, indiquer la configuration D ou L est généralement considéré comme suffisant. Cependant, dans les cas où la direction de la rotation optique doit être spécifiquement soulignée, un signe (+) ou (−) peut être ajouté devant le nom de la molécule. Ces signes expriment des informations expérimentales utilisées pour indiquer le comportement stéréochimique et les propriétés optiques de la molécule.
Les monosaccharides tels que le glucose n’existent pas sous une seule forme cyclique en solution aqueuse. Les molécules s’interconvertissent continuellement entre les anomères α et β par des ouvertures et fermetures répétées du cycle. À la suite de ce processus, la valeur de rotation optique de la solution change avec le temps et atteint finalement une valeur constante. Le phénomène dans lequel la rotation optique change au cours du temps puis atteint une valeur d’équilibre est appelé “mutarotation.”
La rotation optique d’une solution fraîchement préparée de α-D-glucose est d’environ +112°. Cependant, avec le temps, la rotation optique de la solution diminue jusqu’à +52,7° et se fixe à cette valeur. Cela se produit pour la raison suivante : le α-D-glucose présent en solution subit continuellement une ouverture du cycle, et lorsque le cycle se referme, la nouvelle structure de la molécule peut être soit α, soit β. Le β-D-glucose possède une rotation optique d’environ +18,7°. Par conséquent, à mesure que la proportion de la forme β de la molécule augmente dans la solution, le degré de rotation optique de la solution diminue. Lorsque l’équilibre entre les deux formes est établi, la rotation optique de la solution se stabilise à +52,7°. À partir de cette valeur de rotation optique à l’équilibre, on calcule que la solution contient environ 64 % de β-D-glucopyranose et environ 36 % de α-D-glucopyranose.
En conséquence, tandis que la rotation optique révèle la structure chirale et les propriétés stéréochimiques des monosaccharides, la mutarotation montre le comportement d’équilibre dynamique de ces molécules en solution. Ensemble, ces deux propriétés jouent un rôle important dans la compréhension des propriétés chimiques et biologiques des monosaccharides.
2. Isomérie des monosaccharides
Les informations acquises jusqu’à présent rendent nécessaire une explication générale et collective de l’isomérie des monosaccharides. En effet, nous avons mentionné de nombreux types différents d’isomérie, et ils sont très susceptibles d’être confondus les uns avec les autres.
Comme les monosaccharides contiennent plus d’un atome de carbone chiral dans leur structure, ils peuvent former de nombreux isomères. Les molécules qui possèdent la même formule moléculaire mais diffèrent par leur structure ou par leur arrangement spatial sont appelées isomères. Les isomères sont généralement divisés en deux grands groupes: les isomères structuraux (constitutionnels) et les stéréoisomères.
2.1. Isomères structuraux (constitutionnels)
Dans les isomères structuraux, l’organisation des liaisons entre les atomes des molécules est différente. En d’autres termes, la manière dont les atomes sont liés les uns aux autres a changé. Dans les monosaccharides, cette situation résulte généralement de la position différente du groupe carbonyle.
Par exemple, le glucose et le fructose possèdent la même formule moléculaire (C₆H₁₂O₆). Cependant, le glucose est un aldose, tandis que le fructose est un cétose. Par conséquent, la position du groupe carbonyle est différente, et ces deux sucres sont des isomères structuraux.
2.2. Stéréoisomères
Dans les stéréoisomères, l’organisation des liaisons des molécules est la même, mais l’arrangement spatial des atomes est différent. Les stéréoisomères sont divisés en deux grands groupes : les énantiomères et les diastéréoisomères.
2.2.1. Énantiomères
Les énantiomères sont des stéréoisomères qui sont des images miroir l’une de l’autre. Ces molécules possèdent les mêmes propriétés physiques dans un environnement achiral, c’est-à-dire en l’absence d’un réactif chiral ou d’une interaction chirale dans l’environnement, mais elles font tourner la lumière polarisée plane dans des directions opposées. Dans les glucides, l’énantiomérie est généralement exprimée par la désignation D et L. Par exemple, le D-glucose et le L-glucose sont des énantiomères l’un de l’autre.
Un point doit être particulièrement souligné ici. Le fait que seul l’atome de carbone chiral portant le numéro le plus élevé soit pris en compte lors de la détermination de la désignation D et L ne signifie pas que la différence entre les deux molécules réside uniquement dans cet atome de carbone. Le système D et L n’est qu’une méthode de classification. Dans ce système, le fait qu’une molécule appartienne à la série D ou L est déterminé selon la position du carbone pris comme référence.
En réalité, cependant, dans deux molécules qui sont des énantiomères, la configuration de tous les centres chiraux est opposée. Par exemple, lorsque l’on compare le D-glucose et le L-glucose, la différence ne se situe pas uniquement au niveau du carbone C5 ; l’arrangement stéréochimique de tous les carbones C2, C3, C4 et C5 est l’image miroir de l’autre molécule. Cependant, dans la classification D/L, seul le carbone chiral portant le numéro le plus élevé est pris comme référence. Ainsi, la désignation D et L n’exprime pas toutes les différences stéréochimiques entre les deux molécules, mais plutôt un système pratique de dénomination indiquant simplement à quelle série elles appartiennent.
2.2.2. Diastéréoisomères
Les diastéréoisomères sont des stéréoisomères qui ne sont pas des images miroir les uns des autres. Les propriétés physiques et chimiques de ces molécules sont généralement différentes.
2.2.2.1. Épimères
Un sous-groupe particulier des diastéréoisomères est appelé épimères. Les épimères sont des diastéréoisomères dont la configuration diffère au niveau d’un seul atome de carbone chiral. Par exemple, le D-glucose et le D-mannose sont des épimères en C2 l’un de l’autre. Le D-glucose et le D-galactose sont des épimères en C4 l’un de l’autre.
2.2.2.2. Anomères
Lorsque les monosaccharides forment un cycle, le carbone carbonylé devient un nouveau centre chiral. Ce carbone est appelé carbone anomérique. Les isomères formés selon la configuration du carbone anomérique sont appelés anomères. Par exemple, le α-D-glucose et le β-D-glucose sont des anomères l’un de l’autre.
J’explique généralement l’isomérie des monosaccharides à mes étudiants de la manière suivante:
Pensez aux deux mains d’une personne;
• Dans des conditions normales, les deux mains possèdent la même structure; les deux mains ont des doigts, les points d’attache des doigts sont les mêmes et les deux mains sont l’image miroir l’une de l’autre. Dans ce cas, les deux mains sont des énantiomères l’une de l’autre. Le D-glucose et le L-glucose sont ainsi.
• Maintenant, imaginez que dans l’une des deux mains, le pouce ne sorte pas de son emplacement normal, mais qu’il sorte plutôt de la paume. Dans ce cas, la structure a changé. La même paume, les mêmes doigts, les mêmes composants; mais dans une main, contrairement à l’autre, l’un des doigts sort de la paume. Nous ne pouvons plus parler de deux mains qui sont des images miroir l’une de l’autre. Dans ce cas, ces deux mains sont des isomères structuraux l’une de l’autre. Le glucose et le fructose sont ainsi.
• Maintenant, imaginez que dans l’une des deux mains, l’index soit plié vers l’avant, tandis que dans l’autre main, l’index soit plié vers l’arrière. La même paume, les mêmes doigts, et attachés à la paume aux mêmes points; cependant, les positions des index sont différentes. Dans ce cas également, ces deux mains ne sont plus des images miroir l’une de l’autre. Ces deux mains sont des épimères l’une de l’autre. Le glucose et le galactose sont ainsi.
• Maintenant, imaginez que dans l’une des deux mains, l’ongle du pouce soit très long et courbé vers l’avant, tandis que dans l’autre main, l’ongle du pouce soit également très long mais courbé vers l’arrière. Dans ce cas, tout est identique, mais les directions des ongles du pouce sont différentes. Ces deux mains sont des anomères l’une de l’autre. Le α-D-glucose et le β-D-glucose sont ainsi.
Dans le tableau ci-dessous, la classification de l’isomérie des monosaccharides et certaines propriétés importantes sont présentées;
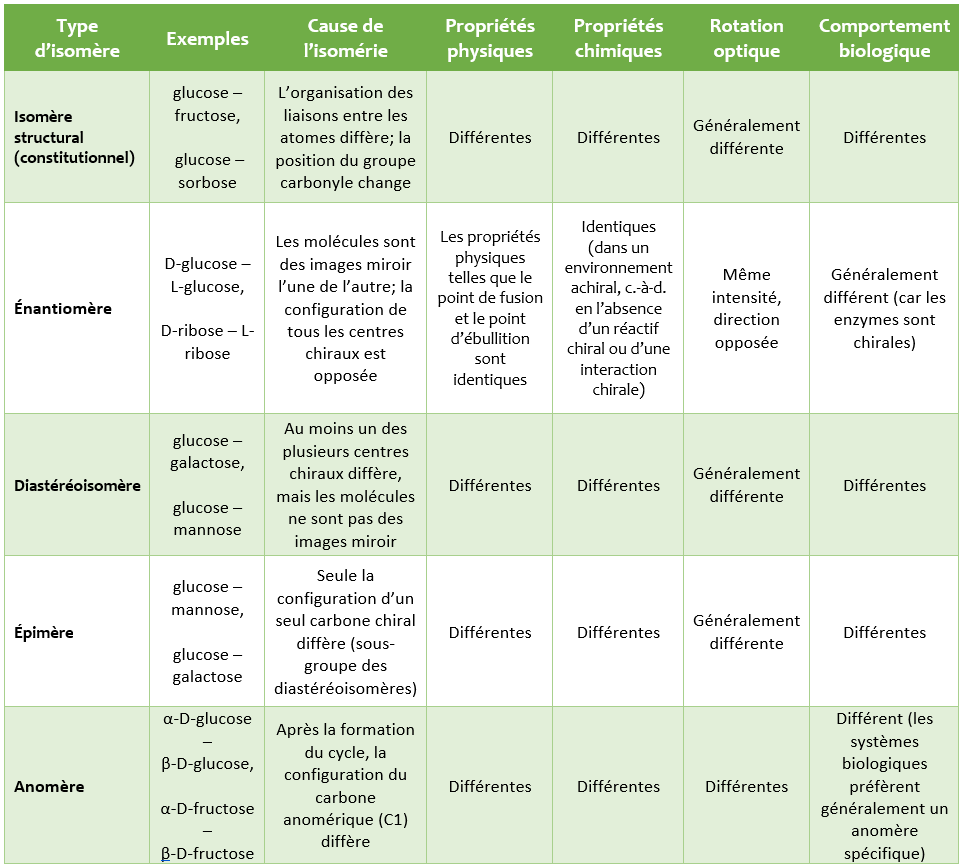
À ce stade, la pensée suivante peut surgir: “Puisque le glucose et le galactose possèdent la même formule moléculaire, ce sont des isomères structuraux.” Cependant, cette idée n’est pas correcte. Car pour qu’une molécule soit considérée comme un isomère structural, il ne suffit pas simplement qu’elle possède la même formule moléculaire; l’organisation des liaisons entre les atomes doit également être différente.
Si l’organisation des liaisons entre les atomes a changé entre les isomères, il s’agit d’isomérie structurale (constitutionnelle); si l’organisation des liaisons reste identique et que seul l’arrangement spatial des atomes change, il s’agit de stéréoisomérie. Par exemple, bien que le glucose et le fructose possèdent la même formule moléculaire (C₆H₁₂O₆), ils sont des isomères structuraux parce que la position du groupe carbonyle est différente. En revanche, dans le glucose et le galactose, l’organisation des liaisons entre les atomes est identique; la différence provient uniquement de l’arrangement spatial des groupes hydroxyles sur certains carbones chiraux. Par conséquent, le glucose et le galactose ne sont pas des isomères structuraux, mais des stéréoisomères.
En résumé, “avoir la même formule moléculaire” ne signifie pas à lui seul qu’il existe une isomérie structurale. Ce qui est déterminant, c’est la manière dont les atomes sont liés les uns aux autres.
Une autre règle importante qui détermine le nombre d’isomères dans les monosaccharides est le nombre d’atomes de carbone chiraux que possède la molécule. Si une molécule contient n atomes de carbone chiraux, le nombre maximal de stéréoisomères pouvant théoriquement se former est 2ⁿ. La raison en est que chaque atome de carbone chiral peut adopter deux configurations différentes. Par exemple, si une molécule possède deux carbones chiraux, théoriquement 2² = 4 stéréoisomères différents peuvent se former; si elle possède trois carbones chiraux, théoriquement 2³ = 8 stéréoisomères différents peuvent se former. Cette règle s’applique également aux monosaccharides.
Par exemple, puisque les aldohexoses possèdent quatre atomes de carbone chiraux (C2, C3, C4 et C5) dans leur forme linéaire ouverte, théoriquement 2⁴ = 16 stéréoisomères différents peuvent se former. La moitié de ces isomères appartient à la série D et l’autre moitié à la série L. Le glucose, le galactose et le mannose ne sont que quelques exemples représentant ces isomères. Ainsi, les monosaccharides que nous rencontrons dans la nature ne représentent qu’une petite partie des stéréoisomères théoriquement possibles.