El tema de la estructura de anillo y el isomerismo en los monosacáridos es uno de los temas más problemáticos en la química de los alimentos, porque contiene una gran cantidad de detalles, incluye muchos términos y, en particular, porque los diferentes isómeros con mucha frecuencia se confunden entre sí.
Dada la importancia del tema, en este artículo intentaré explicar tanto las estructuras de anillo como el isomerismo de los monosacáridos de una manera detallada y comprensible. En la primera parte del artículo se explica la estructura de anillo de los monosacáridos. En la segunda parte, que aparece más abajo, intentaré explicar el isomerismo en los monosacáridos y la clasificación de este isomerismo.
1. La estructura de anillo de los monosacáridos
En la proyección de Fischer, la estructura de los monosacáridos parece presentarse en forma de cadena recta (véase Carbohidratos; Monosacáridos, Disacáridos y Polisacáridos). Sin embargo, aunque esta estructura teórica de cadena recta es correcta, los monosacáridos que contienen cinco o más átomos de carbono en su cadena se encuentran en forma de anillo en condiciones naturales.
Como es sabido, los monosacáridos —ya sean aldosas o cetosas— contienen un grupo carbonilo (C=O) y más de un grupo hidroxilo (-OH) en su estructura. Como puede recordarse de la química orgánica, el grupo carbonilo es electrófilo.
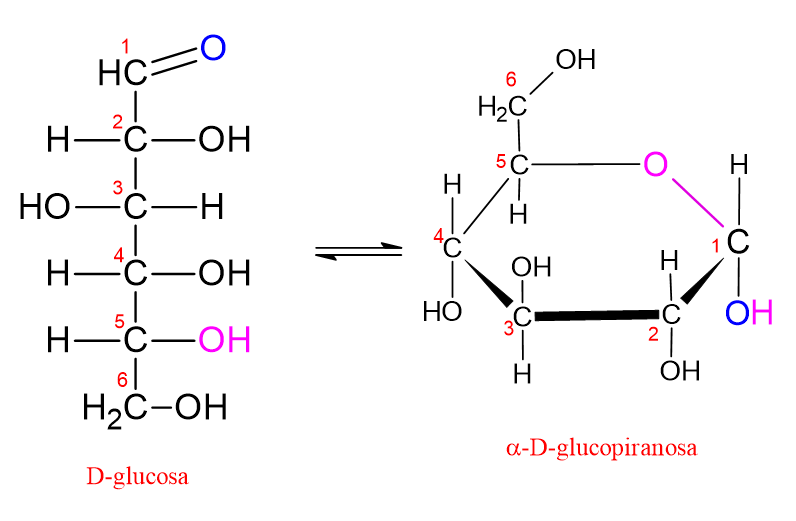
En estas circunstancias, uno de los grupos hidroxilo presentes en la estructura de los monosacáridos (generalmente los grupos -OH unidos a los átomos de carbono C5 o C4) realiza un ataque nucleofílico al grupo carbonilo en la misma cadena. El par de electrones no compartidos del átomo de oxígeno del grupo -OH ataca al átomo de carbono del grupo carbonilo.
Como resultado, se forma un enlace covalente (C–O) entre el oxígeno unido al grupo hidroxilo y el átomo de carbono del grupo carbonilo, y la estructura de cadena recta se convierte en una estructura de anillo.
Para describirlo en el lenguaje de la química, el grupo carbonilo y el grupo hidroxilo sufren una reacción intramolecular y forman un hemiacetal o un hemicetal.
En la proyección de Fischer, las formas D y L de los monosacáridos pueden mostrarse fácilmente en la estructura de cadena recta. Sin embargo, para mostrar la estructura de anillo y las nuevas formas estereoisoméricas de manera comprensible se utilizan las fórmulas de Haworth.
Las fórmulas de Haworth se han utilizado durante más de cien años para representar claramente en el papel la estructura tridimensional del anillo. En la fórmula de Haworth, el plano se considera horizontal. Los enlaces dibujados con líneas más gruesas que los demás indican que esa parte de la molécula está más cerca del observador.
En general, las fuentes de referencia explican las estructuras de anillo de los monosacáridos con afirmaciones como “los monosacáridos con 5 o más átomos de carbono presentan estructura de anillo en medios acuosos o en soluciones.” Sin embargo, esta explicación es bastante propensa a malentendidos y resulta engañosa en el significado que sugiere.
Porque a partir de esta afirmación se puede inferir que los monosacáridos presentan estructura de anillo únicamente en ambientes acuosos, mientras que en forma cristalina y seca permanecen en la forma abierta de cadena recta. En realidad, los monosacáridos con 5 o más átomos de carbono existen en forma de anillo en casi todas las condiciones y en casi todos los entornos. Tomando la glucosa como ejemplo, la glucosa se produce en la planta en forma de cadena abierta, pero en el ambiente celular adopta inmediatamente la estructura de anillo, en milisegundos después de su formación.
Por otra parte, la forma abierta de cadena recta y la forma de anillo de los monosacáridos se encuentran en un estado constante de interconversión. Por ejemplo, en una solución acuosa de glucosa, la molécula de glucosa pasa continuamente de la forma abierta de cadena recta a la forma de anillo y viceversa. Sin embargo, en cualquier momento dado, más del 99 % de la glucosa en solución se encuentra en forma de anillo, mientras que menos del 0,1 % restante se encuentra en la forma abierta de cadena recta. En el estado cristalino seco de la glucosa, casi todas las moléculas se encuentran en forma de anillo y no se produce una transición a la forma abierta de cadena recta como ocurre en medios acuosos. En estructuras más grandes como la sacarosa y el almidón, la glucosa también se encuentra nuevamente en forma de anillo.
Aquí pueden surgir varias preguntas. Intentemos responderlas brevemente.
Pregunta 1: ¿Por qué los monosacáridos con 5 o más átomos de carbono pueden formar estructuras de anillo, mientras que los monosacáridos con menos átomos de carbono no pueden?
Respuesta: Esto está completamente relacionado con la estabilidad y la adecuación. Los monosacáridos con 3 átomos de carbono no son lo suficientemente largos como para formar una estructura de anillo. En los monosacáridos con 4 átomos de carbono, la estructura de anillo que se formaría no sería estable debido a la alta tensión intramolecular.
Pregunta 2: ¿Por qué el grupo hidroxilo no ataca al grupo carbonilo de un monosacárido vecino, sino que ataca a su propio grupo carbonilo?
Respuesta: La razón más importante es la falta de concentración efectiva. Dentro de la molécula, los grupos carbonilo e hidroxilo siempre están cerca uno del otro y se encuentran en la posición geométrica correcta. Para que un grupo de otra molécula se encuentre cerca, en el ángulo correcto y con la energía adecuada, habría que esperar a que ocurra esa situación; esto representa una desventaja considerable. Además, si tal enlace se formara, el resultado sería una molécula muy grande e irregular, lo cual no constituye una vía favorable.
En los monosacáridos con más de 5 átomos de carbono hay dos grupos hidroxilo (-OH) a una distancia adecuada para enlazarse con el átomo de carbono del grupo carbonilo (C=O) durante la formación del anillo: los grupos hidroxilo unidos a C4 y C5.
Expliquemos esto mediante la glucosa, que contiene 6 átomos de carbono en su estructura. En la glucosa, el grupo carbonilo (C=O) se encuentra en el primer carbono (C1). Si el grupo hidroxilo unido al carbono C5 de la cadena ataca al carbono carbonílico, se forma un anillo de seis miembros. Esto se denomina “anillo de piranosa.” Este nombre se le dio porque se asemeja a la molécula de pirano, que es una estructura de anillo de seis miembros que contiene oxígeno.
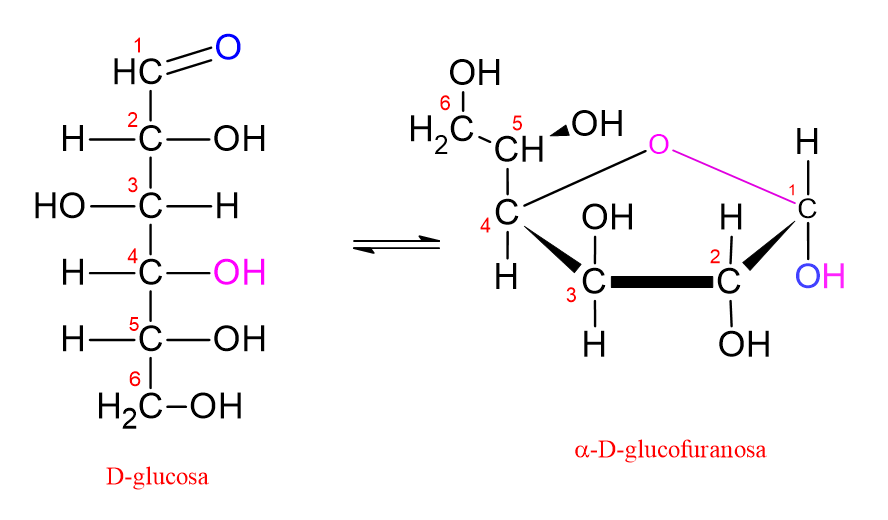
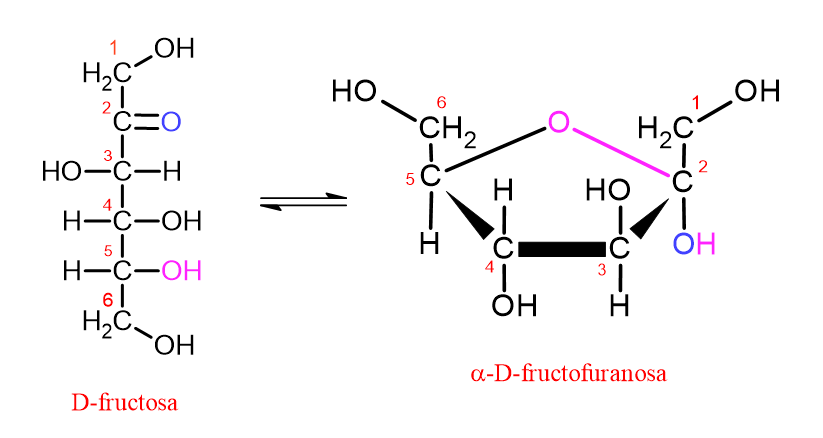
Por el contrario, el grupo hidroxilo en el carbono C4 de la glucosa también se encuentra a una distancia adecuada para reaccionar con el carbono en C1. Si el grupo hidroxilo unido al carbono C4 ataca al carbono carbonílico, entonces se forma un anillo de cinco miembros. Esto se denomina “anillo de furanosa.” Este nombre se le dio porque se asemeja a la molécula de furano, que es una estructura de anillo de cinco miembros que contiene oxígeno.
Como resultado, en los monosacáridos pueden observarse dos tipos diferentes de anillos.
1. Piranosa; estructura de anillo de seis miembros en la que uno de los miembros es oxígeno
2. Furanosa; estructura de anillo de cinco miembros en la que uno de los miembros es oxígeno
Las estructuras de anillo de piranosa y furanosa de algunos monosacáridos se muestran a continuación;
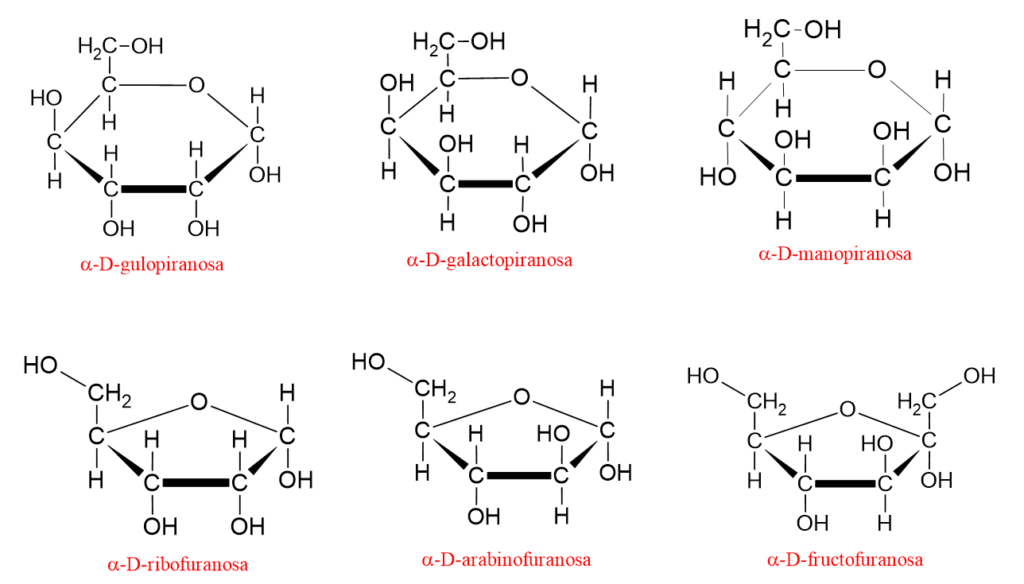
En este punto puede surgir la siguiente pregunta: ¿por qué en los monosacáridos solo se observan estructuras de anillo de 5 y 6 miembros?
Respuesta: Durante la formación del anillo en los monosacáridos, teóricamente pueden formarse anillos de diferentes tamaños. Sin embargo, los anillos que se encuentran con mayor frecuencia en la naturaleza son los de cinco y seis miembros. La razón principal de esto es que los anillos de estos tamaños son químicamente bastante estables.
Como puede recordarse de la química orgánica, la estabilidad de los anillos está en gran medida relacionada con los ángulos de enlace y la tensión intramolecular. Cuando los átomos de carbono tienen hibridación sp³, el ángulo de enlace ideal es aproximadamente de 109,5°. En anillos muy pequeños, este ángulo se distorsiona considerablemente y se genera una alta tensión dentro de la molécula.
Por ejemplo, en anillos de tres o cuatro miembros, los ángulos de enlace se desvían considerablemente del valor ideal. Por esta razón, dichos anillos tienen alta energía y son inestables. En cambio, en anillos de cinco y seis miembros, los ángulos de enlace están más cerca del valor ideal y la tensión intramolecular es mucho menor. Por lo tanto, estos anillos se consideran más estables.
En anillos mayores de seis miembros, la tensión de los ángulos de enlace generalmente no representa un problema importante. Sin embargo, cuando se forman estos anillos, resulta más difícil que la cadena se cierre en la posición correcta. En otras palabras, disminuye la probabilidad de que los extremos de la molécula se encuentren en la posición y el ángulo correctos. Esto hace que la formación del anillo sea cinéticamente menos favorable. Además, como los anillos grandes suelen ser más flexibles, también pueden aparecer tensiones adicionales en ciertas conformaciones.
En resumen;
• Los anillos con menos de 5 miembros no son estables debido a la tensión angular.
• Los anillos de cinco y seis miembros son las estructuras de anillo más estables.
• Los anillos con más de 6 miembros tienen una baja probabilidad de cierre y son propensos a tensiones adicionales.
La tabla siguiente presenta la tendencia general acerca de qué estructura de anillo predomina en qué monosacáridos;

Esta tabla no es una regla absoluta, pero sí muestra una fuerte tendencia. En solución, los monosacáridos existen en un estado de equilibrio dinámico entre diferentes formas de anillo. Por lo tanto, además de la forma de anillo predominante, otras formas de anillo también pueden estar presentes en pequeñas proporciones. Sin embargo, en la mayoría de los monosacáridos este equilibrio favorece claramente una sola forma de anillo.
La estructura de anillo también trae consigo un nuevo centro quiral. Continuando con la glucosa como ejemplo, cuando la glucosa forma una estructura de piranosa, el carbono C1 que contiene el grupo carbonilo también se convierte en un nuevo centro quiral. Este carbono también se denomina carbono asimétrico o carbono anomérico.
En la estructura de cadena recta de la glucosa, la quiralidad de los carbonos es la siguiente:
• C1: no es quiral
• C2: centro quiral
• C3: centro quiral
• C4: centro quiral
• C5: centro quiral
• C6: no es quiral
Al determinar la configuración de la molécula en la estructura de cadena recta, se toma como referencia el carbono quiral con el número de carbono más alto. En este caso, si el grupo hidroxilo (-OH) en el carbono C5 de la glucosa está a la derecha, se expresa como configuración D; si está a la izquierda, se expresa como configuración L.
Sin embargo, con la transición a la estructura de anillo, el carbono C1 también se vuelve quiral. Este carbono ahora se denomina carbono anomérico. Por lo tanto, surgen dos posibilidades adicionales de configuración en la estructura de anillo. Dependiendo de la posición del grupo hidroxilo (-OH) unido a este nuevo carbono quiral, aparecen dos nuevas formas estereoisoméricas en la estructura de anillo: α (alfa) y β (beta).
En la proyección de Fischer, los grupos hidroxilo que se muestran en el lado derecho de la molécula se representan en el lado inferior de la molécula en la fórmula de Haworth. Los que se muestran en el lado izquierdo en la proyección de Fischer se representan en el lado superior en la fórmula de Haworth. En la fórmula de Haworth, si el grupo hidroxilo unido al carbono anomérico (C1) se muestra hacia abajo, la molécula se denomina forma α. Si el grupo hidroxilo unido al carbono anomérico (C1) se muestra hacia arriba, la molécula se denomina forma β. Esto se muestra en la figura siguiente;
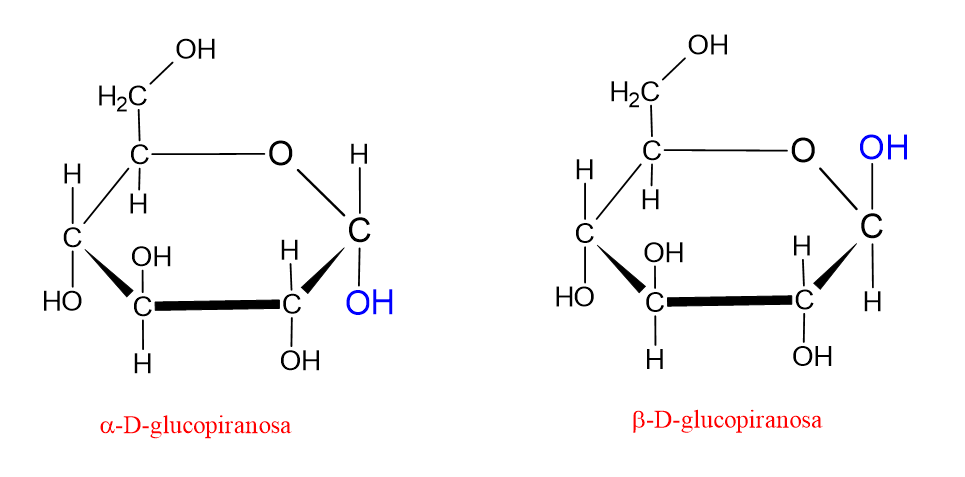
Las proyecciones de Haworth son muy útiles para mostrar claramente la estructura de anillo de los monosacáridos. Sin embargo, esta representación no refleja completamente la verdadera geometría tridimensional de la molécula. En la fórmula de Haworth, el anillo se dibuja como un pentágono o un hexágono plano. En realidad, los átomos de carbono tienen hibridación sp³ y ángulos de enlace de aproximadamente 109,5°. Por esta razón, las moléculas no pueden formar una estructura de anillo perfectamente plana. Para acercar los ángulos de enlace al valor ideal y reducir la tensión intramolecular, la molécula adopta ciertas conformaciones en el espacio.
Los anillos de furanosa de cinco miembros generalmente adoptan conformaciones de sobre y de torsión, mientras que los anillos de piranosa de seis miembros se encuentran en la naturaleza principalmente en conformaciones de silla y de bote. La razón principal de la aparición de estas conformaciones es acercar los ángulos de enlace al ángulo tetraédrico ideal y reducir la tensión intramolecular. Las diferentes conformaciones formadas por los monosacáridos se muestran a continuación;
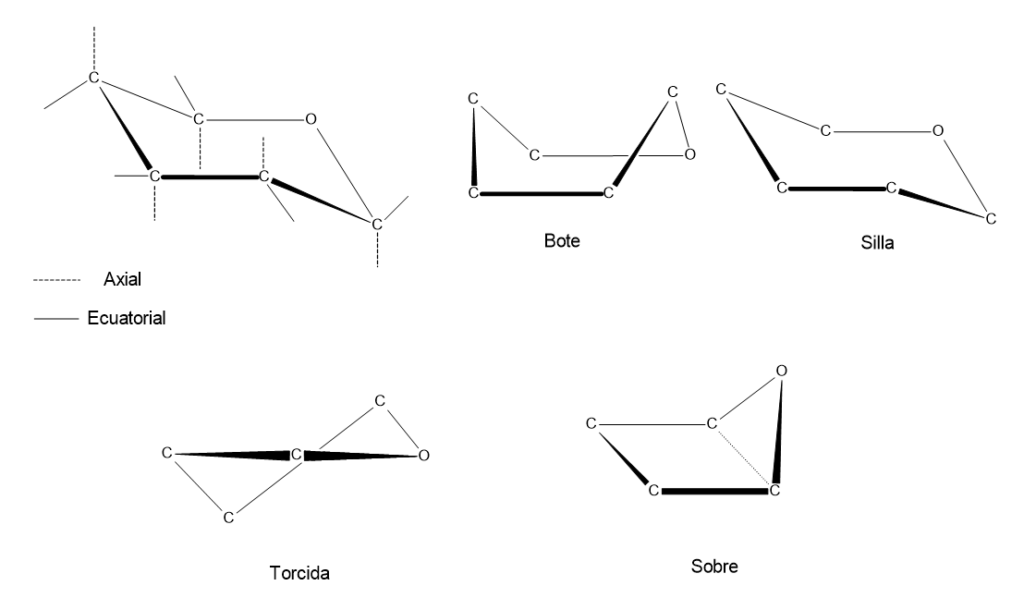
En la conformación de silla, los grupos unidos a cada átomo de carbono del anillo pueden ocupar dos posiciones diferentes en el espacio: axial y ecuatorial. Los enlaces axiales están orientados aproximadamente de manera perpendicular al anillo, ya sea hacia arriba o hacia abajo. Los enlaces ecuatoriales se extienden hacia afuera del anillo en una dirección aproximadamente paralela al plano del anillo.
En general, la posición ecuatorial es más estable. La razón es que los grupos grandes en posición axial crean repulsión estérica con otros grupos axiales del anillo. Por esta razón, átomos pequeños como el hidrógeno pueden ocupar la posición axial, pero los grupos más grandes prefieren la posición ecuatorial.
En resumen, puede afirmarse lo siguiente: en la conformación de silla de los anillos de monosacáridos de seis miembros, la preferencia de los grupos grandes por la posición ecuatorial reduce las interacciones estéricas intramoleculares y aumenta la estabilidad de la estructura.
En la conformación de silla de la β-D-glucopiranosa, casi todos los grupos hidroxilo se encuentran en posición ecuatorial, mientras que solo los átomos de hidrógeno ocupan posiciones axiales. Esto reduce en gran medida la tensión estérica intramolecular y hace que la estructura sea altamente estable. Por lo tanto, la β-D-glucopiranosa es la forma más estable de la glucosa y se encuentra en la mayor proporción en solución.
En este punto podemos decir que hemos completado la explicación de la estructura de anillo de los monosacáridos. Lo que queda es la explicación de la rotación óptica y la mutarrotación en los monosacáridos.
1.1. Rotación óptica y mutarrotación en los monosacáridos
Debido a que los monosacáridos contienen más de un átomo de carbono quiral, son ópticamente activos. Las moléculas ópticamente activas tienen la propiedad de rotar la luz polarizada en un plano en una determinada dirección. El fenómeno de cambiar la dirección de la luz polarizada se denomina rotación óptica.
Dos estereoisómeros diferentes de una molécula ópticamente activa pueden presentar propiedades físicas y químicas similares. Sin embargo, la dirección y el ángulo con los que estos dos estereoisómeros rotan la luz polarizada son propios de cada uno de ellos. Por esta razón, la actividad óptica se utiliza con frecuencia para distinguir entre los estereoisómeros de una molécula.
Si una molécula rota la luz polarizada en el sentido de las agujas del reloj, se denomina positiva (+) o dextrorrotatoria; si la rota en sentido contrario a las agujas del reloj, se denomina negativa (−) o levorrotatoria.
Un punto importante aquí es que estos signos no pueden predecirse de manera fiable observando la estructura de la molécula. La dirección en la que una molécula rota la luz polarizada generalmente se determina experimentalmente mediante mediciones realizadas con un instrumento llamado polarímetro. Por lo tanto, el signo (+) o (−) colocado antes del nombre de una molécula no indica una predicción teórica, sino una propiedad determinada experimentalmente.
Otro punto importante respecto a la rotación óptica es que no debe confundirse con la designación D y L. El sistema D y L expresa la configuración de la molécula y se determina según la posición de un carbono quiral específico en la proyección de Fischer. En cambio, los signos (+) y (−) muestran la dirección en la que la molécula rota la luz polarizada. Por lo tanto, no existe una relación directa entre la configuración D o L y la dirección de la rotación óptica. Por ejemplo, la glucosa generalmente se expresa como D-(+)-glucosa, mientras que la fructosa puede representarse como D-(−)-fructosa. Como puede verse, aunque ambas moléculas están en configuración D, sus direcciones de rotación óptica son diferentes.
Por último, al nombrar una molécula, escribir el signo (+) o (−) a menudo no es obligatorio. En la identificación de los monosacáridos, indicar la configuración D o L generalmente se considera suficiente. Sin embargo, en los casos en que la dirección de la rotación óptica debe enfatizarse específicamente, puede añadirse un signo (+) o (−) antes del nombre de la molécula. Estos signos expresan información experimental utilizada para indicar el comportamiento estereoquímico y las propiedades ópticas de la molécula.
Los monosacáridos como la glucosa no existen en una única forma de anillo en solución acuosa. Las moléculas se interconvierten continuamente entre los anómeros α y β mediante la apertura y el cierre repetidos del anillo. Como resultado de este proceso, el valor de rotación óptica de la solución cambia con el tiempo y finalmente alcanza un valor constante. El fenómeno en el que la rotación óptica cambia con el tiempo y alcanza un valor de equilibrio se denomina mutarrotación.
La rotación óptica de una solución recién preparada de α-D-glucosa es aproximadamente +112°. Sin embargo, con el tiempo, la rotación óptica de la solución disminuye hasta +52,7° y se fija en ese valor. Esto ocurre por la siguiente razón: la α-D-glucosa en solución sufre continuamente apertura del anillo y, cuando el anillo vuelve a cerrarse, la nueva estructura de la molécula puede ser α o β. La β-D-glucosa tiene una rotación óptica de aproximadamente +18,7°. Por lo tanto, a medida que aumenta la proporción de la forma β de la molécula en solución, el grado de rotación óptica de la solución disminuye. Cuando se establece el equilibrio entre las dos formas, la rotación óptica de la solución se fija en +52,7°. A partir de este valor de rotación óptica en equilibrio, se calcula que la solución contiene aproximadamente 64% β-D-glucopiranosa y aproximadamente 36% α-D-glucopiranosa.
Como resultado, mientras que la rotación óptica revela la estructura quiral y las propiedades estereoquímicas de los monosacáridos, la mutarrotación muestra el comportamiento de equilibrio dinámico de estas moléculas en solución. Juntas, estas dos propiedades desempeñan un papel importante en la comprensión de las propiedades químicas y biológicas de los monosacáridos.
2. Isomerismo en los monosacáridos
La información adquirida hasta ahora hace necesaria una explicación general del isomerismo en los monosacáridos. Esto se debe a que hemos mencionado muchos tipos diferentes de isomerismo, y es bastante fácil confundirlos entre sí.
Debido a que los monosacáridos contienen más de un átomo de carbono quiral en su estructura, pueden formar muchos isómeros. Las moléculas que tienen la misma fórmula molecular pero difieren en su estructura o en su disposición espacial se denominan isómeros. Los isómeros generalmente se dividen en dos grupos principales: isómeros estructurales (constitucionales) y estereoisómeros.
2.1. Isómeros estructurales (constitucionales)
En los isómeros estructurales, la disposición de los enlaces entre los átomos de las moléculas es diferente. En otras palabras, la forma en que los átomos están conectados entre sí ha cambiado. En los monosacáridos, esta situación generalmente surge debido a la diferente posición del grupo carbonilo.
Por ejemplo, la glucosa y la fructosa tienen la misma fórmula molecular (C₆H₁₂O₆). Sin embargo, la glucosa es una aldosa, mientras que la fructosa es una cetosa. Por lo tanto, la posición del grupo carbonilo es diferente y estos dos azúcares son isómeros estructurales.
2.2. Estereoisómeros
En los estereoisómeros, la disposición de los enlaces de las moléculas es la misma, pero la disposición espacial de los átomos es diferente. Los estereoisómeros se dividen en dos grupos principales: enantiómeros y diastereómeros.
2.2.1. Enantiómeros
Los enantiómeros son estereoisómeros que son imágenes especulares entre sí. Estas moléculas tienen las mismas propiedades físicas en un entorno aquiral, es decir, en ausencia de un reactivo quiral o de una interacción quiral en el entorno, pero rotan la luz polarizada en direcciones opuestas. En los carbohidratos, el enantiomerismo generalmente se expresa mediante la designación D y L. Por ejemplo, D-glucosa y L-glucosa son enantiómeros entre sí.
Un punto debe enfatizarse aquí en particular. El hecho de que solo se considere el átomo de carbono quiral con el número más alto al determinar la designación D y L no significa que la diferencia entre las dos moléculas se encuentre únicamente en ese átomo de carbono. El sistema D y L es simplemente un método de clasificación. En este sistema, si la molécula pertenece a la serie D o a la serie L se determina según la posición del átomo de carbono utilizado como referencia.
En realidad, en dos moléculas que son enantiómeros, la configuración de todos los centros quirales es opuesta entre sí. Por ejemplo, cuando se comparan D-glucosa y L-glucosa, la diferencia no está solo en el carbono C5; la disposición estereoquímica en los carbonos C2, C3, C4 y C5 es la imagen especular de la otra molécula. Sin embargo, en la clasificación D/L solo se toma como referencia el carbono quiral con el número más alto. Por lo tanto, la designación D y L no expresa todas las diferencias estereoquímicas entre las dos moléculas, sino que constituye un sistema práctico de denominación que indica únicamente a qué serie pertenecen.
2.2.2. Diastereómeros
Los diastereómeros son estereoisómeros que no son imágenes especulares entre sí. Las propiedades físicas y químicas de estas moléculas generalmente son diferentes.
2.2.2.1. Epímeros
Un subgrupo especial de diastereómeros se denomina epímeros. Los epímeros son diastereómeros cuya configuración difiere en un solo átomo de carbono quiral. Por ejemplo, D-glucosa y D-manosa son epímeros en C2 entre sí. D-glucosa y D-galactosa son epímeros en C4 entre sí.
2.2.2.2. Anómeros
Cuando los monosacáridos forman un anillo, el carbono carbonílico se convierte en un nuevo centro quiral. Este carbono se denomina carbono anomérico. Los isómeros formados dependiendo de la configuración del carbono anomérico se denominan anómeros. Por ejemplo, α-D-glucosa y β-D-glucosa son anómeros entre sí.
Suelo explicar el isomerismo en los monosacáridos a mis estudiantes de la siguiente manera:
Piensen en las dos manos de una persona.
• En condiciones normales, las dos manos tienen la misma estructura; ambas manos tienen dedos, los puntos donde se unen los dedos son los mismos y las dos manos son imágenes especulares entre sí. En este caso, las dos manos son enantiómeros entre sí. D-glucosa y L-glucosa son así.
• Ahora imaginen que en una de las dos manos el pulgar no sale de su lugar habitual, sino que sale desde la palma. En este caso la estructura ha cambiado. La misma palma, los mismos dedos, los mismos componentes; pero en una mano, a diferencia de la otra, uno de los dedos sale desde la palma. Ya no podemos hablar de dos manos que sean imágenes especulares entre sí. En este caso, estas dos manos son isómeros estructurales entre sí. La glucosa y la fructosa son así.
• Ahora imaginen que en una de las dos manos el dedo índice está doblado hacia adelante, mientras que en la otra mano el dedo índice está doblado hacia atrás. La misma palma, los mismos dedos y unidos a la palma en los mismos puntos; sin embargo, las posiciones de los dedos índice son diferentes. En este caso también estas dos manos ya no son imágenes especulares entre sí. Estas dos manos son epímeros entre sí. La glucosa y la galactosa son así.
• Ahora imaginen que en una de las dos manos la uña del pulgar es muy larga y está doblada hacia adelante, mientras que en la otra mano la uña del pulgar también es muy larga pero está doblada hacia atrás. En este caso todo es igual, pero las direcciones de las uñas del pulgar son diferentes. Estas dos manos son anómeros entre sí. α-D-glucosa y β-D-glucosa son así.
En la tabla siguiente se presenta la clasificación del isomerismo en los monosacáridos y algunas propiedades importantes;
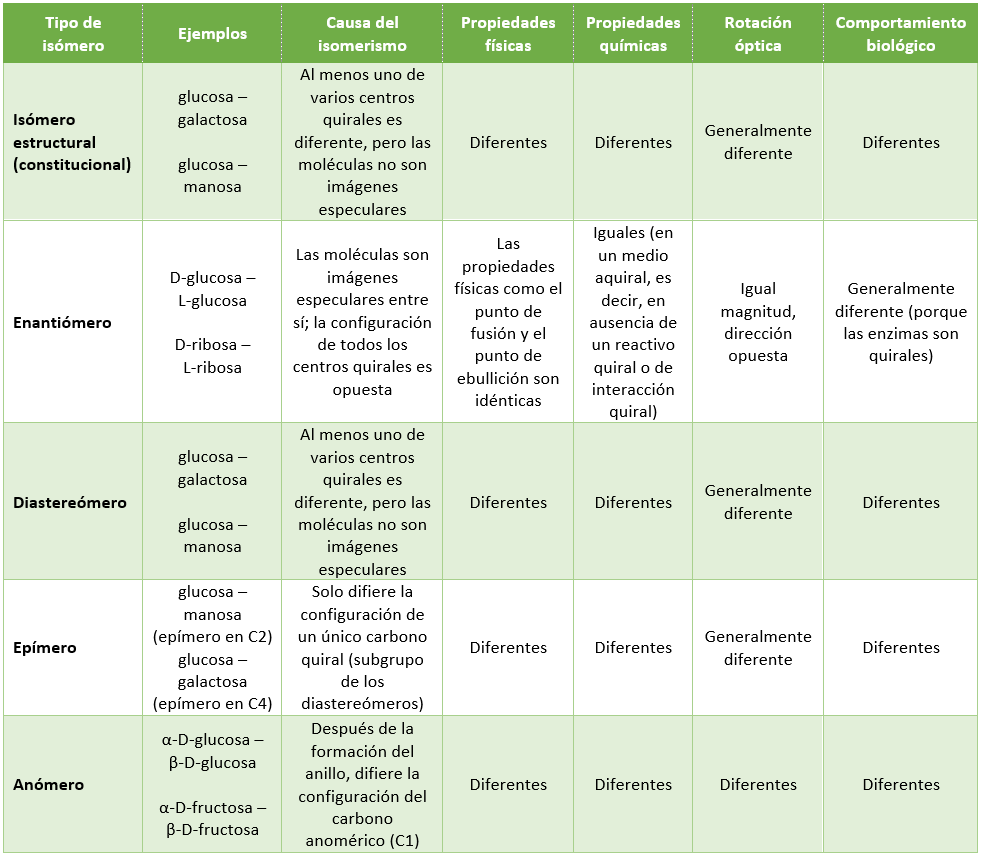
En este punto puede surgir la siguiente idea: “Dado que la glucosa y la galactosa tienen la misma fórmula molecular, son isómeros estructurales.” Sin embargo, esta idea no es correcta. Para que una molécula se considere un isómero estructural no basta con que tenga la misma fórmula molecular; también debe ser diferente la forma en que los átomos están enlazados entre sí.
Si la disposición de los enlaces entre los átomos ha cambiado entre los isómeros, se trata de isomerismo estructural (constitucional); si la disposición de los enlaces permanece igual y solo cambia la disposición espacial de los átomos, se trata de estereoisomerismo. Por ejemplo, aunque la glucosa y la fructosa tienen la misma fórmula molecular (C₆H₁₂O₆), son isómeros estructurales porque la posición del grupo carbonilo es diferente. En cambio, en la glucosa y la galactosa la disposición de los enlaces entre los átomos es la misma; la diferencia surge únicamente de la disposición espacial de los grupos hidroxilo en ciertos carbonos quirales. Por lo tanto, la glucosa y la galactosa no son isómeros estructurales, sino estereoisómeros.
En resumen, tener la misma fórmula molecular por sí solo no significa que exista isomerismo estructural. Lo decisivo es cómo están enlazados los átomos entre sí.
Otra regla importante que determina el número de isómeros en los monosacáridos es el número de átomos de carbono quirales que posee la molécula. Si una molécula contiene n átomos de carbono quirales, el número máximo de estereoisómeros que teóricamente pueden formarse es 2ⁿ. La razón es que cada átomo de carbono quiral puede tener dos configuraciones diferentes. Por ejemplo, si una molécula tiene dos carbonos quirales, teóricamente pueden formarse 2² = 4 estereoisómeros diferentes; si tiene tres carbonos quirales, pueden formarse 2³ = 8 estereoisómeros diferentes. Esta regla también se aplica a los monosacáridos.
Por ejemplo, dado que las aldohexosas tienen cuatro átomos de carbono quirales (C2, C3, C4 y C5) en su forma de cadena abierta, teóricamente pueden formarse 2⁴ = 16 estereoisómeros diferentes. La mitad de estos isómeros pertenece a la serie D y la otra mitad a la serie L. La glucosa, la galactosa y la manosa son solo algunos ejemplos que representan estos isómeros. Por lo tanto, los monosacáridos que encontramos en la naturaleza representan solo una pequeña parte de los estereoisómeros que son teóricamente posibles.