Proteinler organizmaların başlıca yapı malzemesidir. Farklı proteinler farklı işlevlere sahiptir. Eğer vücudu bir bina gibi düşünürsek, binada bulunan demir, tuğla, çimento, pencere ve asansör gibi malzeme ve aksamların her birini organizmada bir protein gibi kabul edebiliriz.
Proteinler ağırlıkla karbon (C), hidrojen (H), oksijen (O), azot (N) ve kükürt (S) elementlerinden oluşmaktadır. Bununla birlikte, proteinlerin yapısında fosfor (P), demir (Fe), bakır (Cu) ve çinko (Zn) da bulunabilmektedir.
Proteinlerin yapıtaşları amino asitlerdir. Sadece amino asitten oluşan proteinler olduğu gibi karbonhidrat ve yağ gibi farklı moleküller de içeren proteinler bulunmaktadır.
Amino asitler
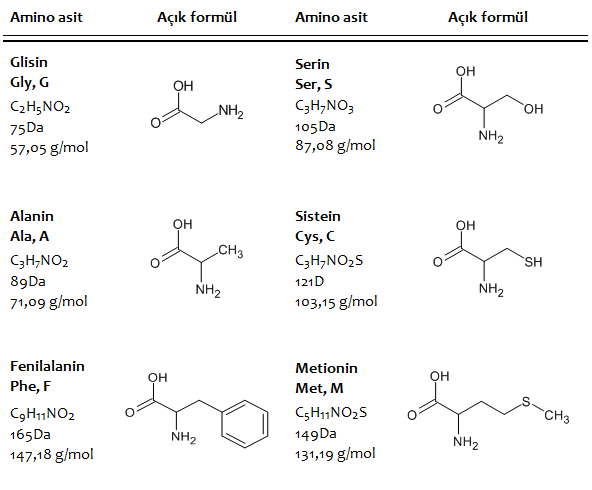
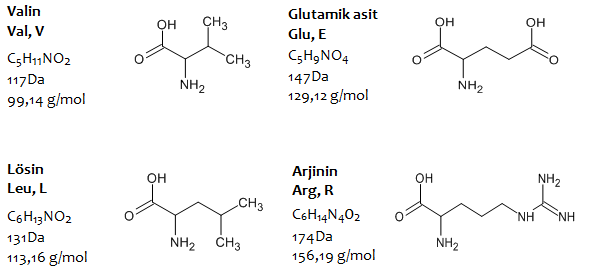
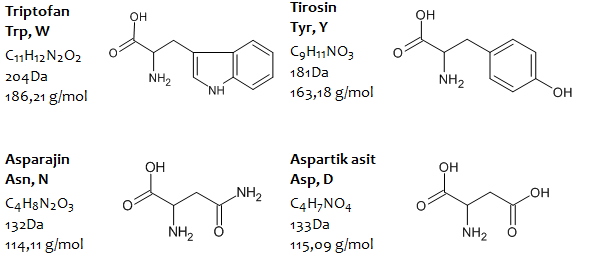
Doğada 200’e yakın amino asit tespit edilmekle birlikte, genellikle bu amino asitlerden 20 tanesi proteinlerin yapısında yer almaktadır.
Amino asitler, yapılarında en az bir adet karboksil grubu (-COOH) ve en az bir adet amino grubu (-NH2) içeren (Prolin imino grubu (–NH) içermektedir), karbon zincirinden oluşmuş moleküllerdir. Zincirdeki karbon sayısı amino asidin çeşidine göre genellikle 2 – 11 arasında değişmektedir.
En basit yapıya sahip amino asit olan glisin, 1 karbon atomuna bir karboksil grubu ve amino grubunun bağlanmasından ibarettir ve 2 karbon atomu içermektedir.

Bir amino asidin karboksil grubu ile diğer amino asidin amino grubu arasında peptit bağı kurularak birleşme sağlanır.
Bu şekilde iki amino asidin birleşmesi sonucu oluşan yapıya dipeptit, üç aminoasidin peptit bağı ile bağlanması ile oluşan yapıya tripeptit denilmektedir. Amino asitler bu şekilde peptit bağı kurarak peptitleri oluşturmaktadırlar.
Proteinler, genellikle 100 veya daha fazla amino asidin birleşmesi ile oluşan peptitlerdir. Bununla birlikte, kimi proteinler 100’den daha az amino asit içermektedir.
Bir proteinin içerdiği amino asit sayısı, zincir uzunluğu ve sırası o proteini üreten organizmanın DNA’sında kodludur. Proteinlerin canlıya özgü oluşu da bundan dolayıdır.
Amino asitlerin birleşerek zincir halini aldığı yapı proteinlerin “primer yapısı” dır. Ancak bu yapı düz zincir halinde kalmaz; zincirdeki aminoasitler birbirleri ile etkileşir ve bu etkileşim sonucu zincirde kıvrımlar meydana gelir.
Etkileşim sonucunda genelde oksijen ve azot arasında hidrojen bağları kurulur. Genellikle 4 amino asitte bir kıvrım gerçekleşmektedir.
Sonuç itibari ile protein bir heliks yapısı kazanır ki; proteinlerin bu yapısına “sekonder yapı” denilmektedir. Miyosin , keratin ve epidermin gibi proteinler sekonder yapıdadır.
Sekonder yapının oluşmasını sağlayan hidrojen bağları zayıf bağlardır, ancak yapıda çok fazla miktarda hidrojen bağı kurulması sekonder yapıyı stabil kılmaktadır.
Bununla birlikte, zincirin kıvrım yerlerinde kükürt içeren iki amino asit karşılıklı denk gelirse bu iki amino asit arasında disülfit bağı (S-S) da kurulmaktadır.
Sekonder yapıda disülfit bağının bulunması yapıyı çok daha sağlam hale getirmektedir. Genel olarak proteinler β-plakalı ve α-heliks olmak üzere iki farklı şekilde sekonder yapı göstermektedir.
Oluşan sekonder yapı da kendi içerisinde hidrojen bağları, disülfit bağları, van der Waals bağları ve hidrofobik etkileşimler göstererek daha karmaşık bir yapıya bürünür. Proteinlerin bu yapısına “tersiyer yapı” denilmektedir. Globüler proteinler genellikle tersiyer yapı göstermektedir.
Birden fazla polipeptit zinciri, söz konusu etkileşimlerle bir araya geldiğinde ise “kuarterner yapı” ortaya çıkmaktadır. Hemoglobin, kuarterner yapıdaki bir proteindir.
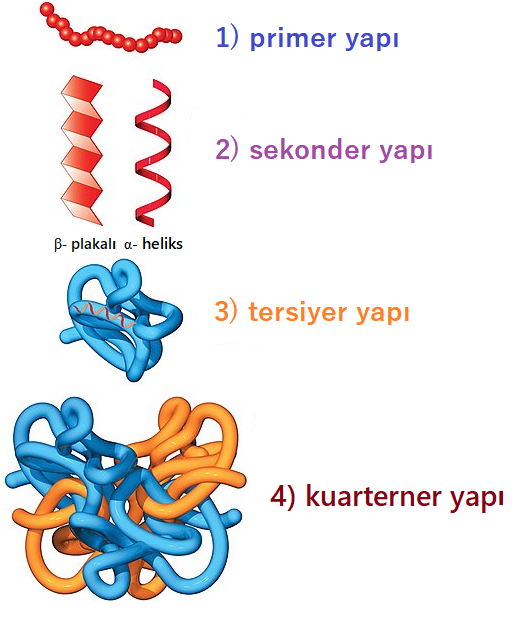
Görsel: Open Oregon – Protein Structure, CC BY 4.0
Doğal olarak her protein içerdiği amino asit sayısına göre, farklı molekül ağırlıklarında olmaktadır. İnsülin 6.000 Da ağırlığında iken, üreaz 480.000 Da ağırlığındadır.
Proteinlerin Sınıflandırılması
Proteinler farklı parametrelere göre sınıflandırılabilmektedir. Bu sınıflandırmalar şu şekildedir;
I) Konfigürasyon tipine göre proteinler;
1. Fibröz proteinler; Suda çözünmeyen çubuk şekilli proteinlerdir. Kollajen, keratin, elastin, tromyosin örnek olarak verilebilir.
2. Globüler proteinler; Suda çözünebilen yuvarlak şekilli proteinlerdir. Serum albümini, hemoglobin, enzimler, antikorlar, hormonlar örnek olarak verilebilir.
II) Kimyasal kompozisyonuna göre proteinler;
1. Basit proteinler; Hidrolize uğradıklarında açığa yalnızca amino asit ve türevleri çıkan proteinlerdir. Albüminler, globülinler, glutelinler, prolaminler, protaminler, histonlar, kollajen, keratin, fibrin, miyosin, elastin, epidermin örnek olarak verilebilir.
2. Bileşik proteinler; Hidrolize uğradıklarında amino asit ve türevlerinin dışında da maddeler açığa çıkaran proteinlerdir. Fosfoproteinler, lipoproteinler, glikoproteinler, nükleoproteinler, kromoproteinler, metaloproteinler örnek olarak verilebilir.
III) İşlevlerine göre proteinler;
1. Enzimler; amilaz, laktaz örnek olarak verilebilir.
2. Yapısal; glikoproteinler, lipoproteinler örnek olarak verilebilir.
3. Kontraktil; myosin, aktin, tubulin örnek olarak verilebilir.
4. Hormonlar; insülin, büyüme hormonları örnek olarak verilebilir.
5. Taşıyıcı; hemoglobin, transferrin, serum albümini örnek olarak verilebilir.
6. Depo; Hardein, gliadin örnek olarak verilebilir.
7. Koruyucu; antikorlar, immünoglobulinler örnek olarak verilebilir.
8. Toksik; yılan zehri, risin örnek olarak verilebilir.
Bu yazıyı da okumak isteyebilirsiniz; Proteinler; Vücuttaki Görevleri, Kalitesi ve Günlük İhtiyaç